العناصر الفلزية واللافلزية
العناصر الفلزية
تُعرَّف العناصر الفلزية، أو الفلزات (بالإنجليزية: METALS) بأنها العناصر التي تميل لأن تكون موصلات كهربائية وحرارية عالية الكفاءة، والتي تتميز بلمعانها، ومرونتها، وقابليتها للإنحناء لتكوين أشكال مختلفة دون أن تنكسر، وتشكّل الفلزات معظم العناصر الموجودة في الجدول الدوري، حيث تشكّل حوالي 80% من مجموعها.[1]
خصائص العناصر الفلزية
تتميز العناصر الفلزية بالعديد من الخصائص، منها ما يأتي:[1]
- تعدّ الفلزات عناصر متينة جداً على الرغم من مرونتها، وتمتلك نقاط انصهار، وغليان عالية.
- تميل العناصر الفلزية إلى تكوين أيونات موجبة عن طريق فقد الإلكترونات.
- تتكون الروابط الأيونية بين العناصر الفلزية نفسها، أو بينها وبين العناصر اللافلزية، وتعدّ الروابط الأيونية أقوى أنواع الروابط الكيميائية، كما توجد روابط كيميائية داخلية قوية جداً بين ذرات الفلز نفسه، مما يجعل من الصعب فصل ذرات الفلزات.
- تمتلك العناصر الفلزية القدرة على تشكيل السبائك، والتي تعدّ خليطاً من واحد أو أكثر من الفلزات.
- تشكّل الفلزات أو المعادن مكونات مهمة لجسم الإنسان، ومن الأمثلة عليها الكالسيوم بنسبة 1.4%، والذي يعدّ خامس العناصر وفرةً في الجسم، والمغنيسيوم بنسبة 0.50%، وهو العنصر السابع وفرة في الجسم، والبوتاسيوم بنسبة 0.34%، والصوديوم بنسبة 0.14%، والحديد بنسبة 0.004%، والزنك الذي يشكل نسبة 0.003%.
- تشكّل الفلزات قسماً كبيراً من العناصر التي توجد في القشرة الأرضية، والغلاف الجوي، والمياه، وفيما يأتي أكثر الفلزات المتوفرة على سطح الأرض:
- يشكّل الألمنيوم ثالث العناصر وفرةً على الأرض بنسبة 7.5%.
- يعدّ الحديد رابع العناصر وفرةً على الأرض بنسبة 4.71%.
- الكالسيومهو العنصر الخامس من حيث الوفرة على الأرض، وبنسبة 3.39%
- الصوديوم هو سادس العناصر المتوفرة على الأرض بنسبة 2.63%.
- يعدّ البوتاسيوم سابع العناصر وفرةً على الأرض بنسبة 2.4%.
- يعدّ المغنيسيوم ثامن العناصر وفرةً على الأرض بنسبة 1.93%.
- يشكّل التيتانيوم نسبة 0.58% على سطح الأرض.
- يشكّل المنغنيز نسبة 0.09% على سطح الأرض.
مجموعات العناصر الفلزية
تُصنّف مجموعات العناصر الفلزية في الجدول الدوري كما يأتي:[2]
- الفلزات القلوية: تشكّل الفلزات القلوية عناصر المجموعة الأولى التي توجد على يسار الجدول الدوري، وتتميز بكثافتها المنخفضة بشكل عام مقارنةً مع الفلزات الأخرى، كما تتميز بشدة تفاعلها، مما يجعلها توجد على شكل مركبات في الطبيعة، ويكون عدد التأكسد لها هو +1، وتضم الفلزات القلوية عناصر الليثيوم، والصوديوم، والبوتاسيوم، والروبيديوم، والسيزيوم، والفرانسيوم، ويعدّ الهيدروجين الموجود في المجموعة الأولى عنصراً غير فلزي في العادة، والذي يوجد بشكل حر في الطبيعة.
- الفلزات القلوية الترابية: تشكّل الفلزات القلوية عناصر المجموعة الثانية في الجدول الدوري، والتي تتميز بلمعانها، وصلابتها، ومرونتها، وقابليتها للطرق، وتمتلك هذه العناصر عدد أكسدة يساوي +2، وتضم هذه المجموعة البريليوم، والمغنيسيوم، والكالسيوم، والسترونتيوم، والباريوم، والراديوم.
- الفلزات الأساسية: تشكّل هذه المجموعة العناصر التي ترتبط عادةّ بمصطلح الفلزات في أذهان الناس، وتعدّ هذه الفلزات موصلات للحرارة والكهرباء، وتتميز ببريقها المعدني، وميلها لأن تكون كثيفةً، وطيعةً، ولدنة، ومن الأمثلة عليها الألمنيوم، والغاليوم، والإنديوم، والثاليوم.
- الفلزات الانتقالية: تمتلك الفلزات الانتقالية حالات أكسدة متعددة، إذ تمتلك مستويات طاقة فرعية f، أو d غير ممتلئة كلياً بالإلكترونات، وقد تتواجد هذه الفلزات في الطبيعة بصورة نقية كالذهب، والفضة، كما قد توجد على شكل مركبات كالأكتينيدات، واللانثانيدات، وتضم الفلزات الانتقالية مجموعةً واسعةً من العناصر، وهي:
- سكانديوم.
- التيتانيوم.
- الفاناديوم.
- الكروم.
- المنغنيز.
- حديد.
- الكوبالت.
- النيكل.
- نحاس.
- زنك.
- الايتريوم.
- الزركونيوم.
- النيوبيوم.
- الموليبدينوم.
- تكنيتيوم.
- الروثينيوم.
- الروديوم.
- البلاديوم.
- الفضة.
- الكادميوم.
- اللنثانوم.
- الهفنيوم.
- التنتالوم.
- التنغستن.
- الرينيوم.
- الأوزميوم.
- إيريديوم.
- البلاتين.
- الذهب.
- الزئبق.
- الأكتينيوم.
- رذرفورديوم.
- دوبنيوم.
- سيبروجيوم.
- بوريوم.
- هاسيوم.
- مايتنريوم.
- دارمشتاتيوم.
- روينتجينيوم.
- كوبرنيسيوم.
- السيريوم.
- البراسيوديميوم.
- النيوديميوم.
- السمريوم.
- الأوروبيوم.
- الغادولينيوم.
- التربيوم.
- الدسبروزيوم.
- هولميوم.
- الأربيوم.
- الثاليوم.
- الايتربيوم.
- اللوتيتيوم.
- الثوريوم.
- البروتكتينيوم.
- اليورانيوم.
- النبتونيوم.
- البلوتونيوم.
- الأمريسيوم.
- الكوريوم.
- البركيليوم.
- كاليفورنيوم.
- الآينشتانيوم.
- الفيرميوم.
- مندليفيوم.
- نوبليوم.
- اللورنسيوم.
العناصر اللافلزية
تُشكّل العناصر اللافلزية أو اللافلزات (بالإنجليزية: Nonmetal) العناصر التي لا تمتلك الخصائص المميزة للفلزات كالصلابة، والموصلية الكهربائية، وتتميز ذرات اللافلزات في العادة بأنها صغيرةً، وتمتلك عدداً كبيراً نسبياً من الإلكترونات في المدارات الخارجية لها، وتشكل العناصر اللافلزية جزءاً كبيراً من القشرة الأرضية على الرغم من عددها القليل، كما تعدّ ضروريةً لنمو الكائنات الحية، وتواجدها.[3]
خصائص العناصر اللافلزية
تتميز العناصر اللافلزية بعدد من الخصائص، منها ما يأتي:[4]
- تمتلك العناصر اللافلزية طاقات تأين عالية، وكهرومغناطيسية عالية أيضاً.
- تعدّ العناصر اللافلزية موصلات كهربائية، وحرارية ضعيفة.
- تشكّل اللافلزات الصلبة مواد هشة، وغير لدنة أو قابلة للطرق.
- تمتلك اللافلزات بريقاً معدنياً منخفضاً جداً، ويكاد يكون معدوماً.
- تكسب العناصر اللافلزية الإلكترونات بسهولة.
- تمتلك اللافلزات نقاط انصهار وغليان منخفضة مقارنةً مع الفلزات.
- قد تكون العناصر الفلزية صلبةً، أو سائلة، أو غازية في درجة حرارة الغرفة.
- تشكّل اللافلزات أكاسيد حمضية.
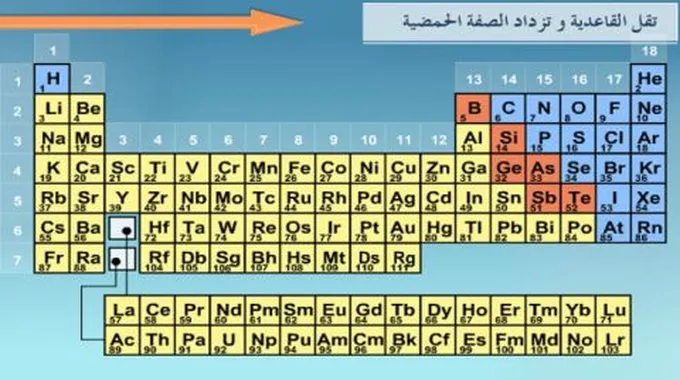
العناصر اللافلزية في الجدول الدوري
توجد معظم العناصر اللافلزية في الجانب الأيمن العلوي من الجدول الدوري باستثناء الهيدروجين الذي يتصرف كلافلز عند درجة حرارة وضغط الغرفة، في حين أنه قد يتصرف كفلز قلوي عند ظروف الضغط المرتفع، وبالإضافة إليه تضم اللافلزات العناصر الآتية:[4]
- الهالوجينات؛ والتي تضم عناصر الفلور، والكلور، والبروم، واليود، والأستاتين، بالإضافة إلى التينيسين، والذي يعتقد معظم العلماء بأنه قد يتصرف كشبه فلز (بالإنجليزية: metalloid).
- الغازات النبيلة، والتي تضم عناصر الهيليوم، والنيون، والآرجون، والزينون، وكريبتون، والرادون، والعنصر رقم 118 (الأوغانسيون)، والذي من المتوقع أن يكون سائلاً.
- تتكون اللافلزات أيضاً من عناصر الكربون، والنيتروجين، والأكسجين، والفسفور، بالإضافة إلى الكبريت، والسيلينيوم.
المراجع
- ^ أ ب "Metals", www.encyclopedia.com, Retrieved 2018-12-27. Edited.
- ↑ Anne Marie Helmenstine (2018-11-19), "Metals: List of Elements"، www.thoughtco.com, Retrieved 2018-12-27. Edited.
- ↑ "Nonmetal", www.britannica.com, Retrieved 2018-12-27. Edited.
- ^ أ ب Anne Marie Helmenstine (2018-9-24), "Nonmetals Definition and Properties"، www.thoughtco.com, Retrieved 2018-12-27. Edited.