خواص الجدول الدوري
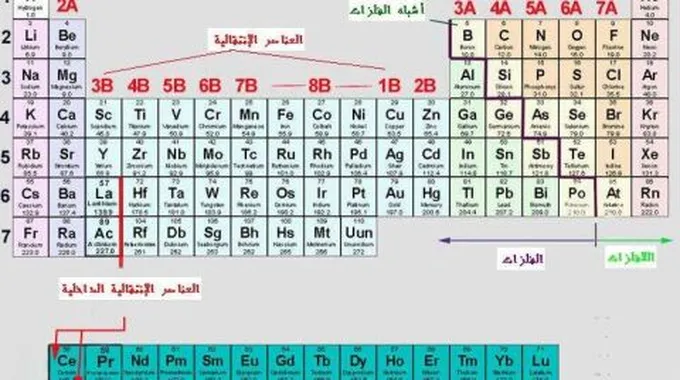
الجدول الدوري
الجدول الدوري له عدة مسميّات ومنها جدول مندليف، والجدول الدوري للعناصر، وهو عبارة عن استعراض لكافة العناصر الكيميائية المعروفة في العالم على شكل جدول، ويعود الفضل في إيجاد هذا الجدول إلى الكيميائي ديمتري مندليف عام 1869م، إذ أقدم على وضع العناصر مرتبة في جدول وفقاً لسلوكها الناتج عنها إثر خصائصها الكيميائية.
تقسيم الجدول الدوري
يُقسّم الجدول إلى مجموعات تتوزّع فيها العناصر البالغ عددها 118 عنصر كيميائي، حيث تصنّف العناصر من 1-98 بأنّها موجودة في الطبيعة، أمّا بقية العناصر من 99-118 فإنّها من صنع الإنسان وتصنع في المختبرات فقط.
خضع الجدول الدوري لتحديثات على يد الكيميائي هنري موزلي عام 1911م، حيث قام بإعادة ترتيب العناصر وفقاً لعددها الذريّ، ومع تقادم الزمن أُحدثت عليه عدة تعديلات بعد كل مرة تُكتشف فيها عناصر جديدة، ومن الجدير بالذكر فإنّ الجدول الدوري يدخل في عدة استخدامات من النواحي الأكاديمية الكيميائيّة، إذ يُقدّم تصنيفاً لكافة الأشكال المتباينة في الخصائص الكيميائيّة وينظمها، ويستخدم في الكيمياء، والفيزياء، والهندسة الكيميائية.
تكمن أهمية الجدول الدوري باستخداماته في مختلف مناحي الحياة للعلماء وطلاب الكيمياء في تقديم تفصيلاً واضحاً للخصائص الكيميائية، والفيزيائية للعناصر الكيميائية، والاختلافات بين المجموعات.
خواص الجدول الدوري
- تتسم عناصر المجموعات الثلاث الأولى بقدرتها على فقد الإلكترونات، أمّا باقي المجموعات فلها قدرة على كسب الإلكترونات.
- يمتاز بانتهاء جميع الدورات بالعناصر الخاملة، أي أن إلكترونات مداره الأخير تكون ممتلئة.
- تحديد رقم الدورة التي ينتمي إليها العنصر الكيميائي بالاعتماد على عدد الإلكترونات الموجودة في مداره الأخير.
- وجود سلسلتي لانثانيدات والأكتنيدات في أسفل الجدول الدولي، وتمتازان بالطول الزائد عن باقي السلاسل، إذ تحتوي كلّ منهما على 14 عنصر كيميائي، وتكون منتمية للعناصر الانتقاليّة.
- تقسيم العناصر الكيميائيّة إلى فلزات ولا فلزات وأشباه فلزات.
التصنيف في الجدول الدوري
بُني الجدول الدوري على هيئة دورات ومجموعات صُنّفت فيها العناصر الكيميائية وفقاً خصائصها التي تتشابه فيها، فيتألّف الجدول من ثمانية عشر مجموعة، وتتشابه العناصر الموجودة في نفس المجموعة في تركيب غلاف التكافؤ، أي يكون لها نفس عدد الإلكترونات تقريباً وبالتالي تتشابه فيما بينها بالخواص الكيميائيّة.
ينفرد الجدول الدوريّ بقدرته على ترتيب العناصر الكيميائية بدقة عالية، إذ تزداد عدد الطبقات كلّما انتقلنا من سطر إلى آخر، كما يزداد عدد الإلكترونات في الطبقة الخارجيّة عند الانتقال من عمود إلى آخر، وتُرّقم المجموعات وفقاً لثلاثة أنظمة وهي الأرقام العربيّة، والرومانيّة، والحروف اللاتينيّة، وقد وقّع اختبار الترقيم وفقاً للأرقام العربيّة من قِبل الاتحاد الدولي للكيمياء والكيمياء التطبيقيّة.