تصنيف العناصر في الجدول الدوري
الجدول الدوريالجدول الدوري للعناصر أو جدول مندليف هو عرض للعناصر الكيميائيّة التي تمّ اكتشافها عبر العصور، وتعود هذه الطريقة المتبعة في ترتبيه إلى العالم

الجدول الدوري
الجدول الدوري للعناصر أو جدول مندليف هو عرض للعناصر الكيميائيّة التي تمّ اكتشافها عبر العصور، وتعود هذه الطريقة المتبعة في ترتبيه إلى العالم الروسي ديمتري مندليف جيث قام بتصنيفه في الفترة ما بين عامي 1869م و1870م، حيث قام بالعديد من الحسابات التي توضح كتل العناصر ودوريتها، ثم رتبها بالاعتماد على هذ الحسابات على التوالي، ومع مرور الوقت أضيفت إليه مجموعة من العناصر التي تمّ اكتشافها لاحقاً ليصبح بهذا الشكل الحالي.
تصنيف العناصر في الجدول الدوري
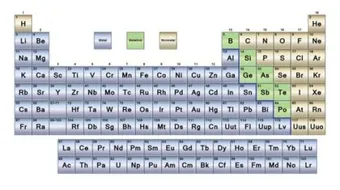
يحتوي الجدول الدوري الحالي على مئة وثمانية عشر عنصراً، مقسمّة إلى ثماني عشرة مجموعة رأسية، وتقسّم العناصر حسب نوعها إلى:
- العناصر النبيلة: أو الغازات النبيلة، وهي العناصر التي تحتوي على عدد مكتمل من الإلكترونات في مداراتها الأخيرة، وبالتالي فهي خاملة في التفاعلات الكيميائية.
- العناصر المثالية: وهي العناصر التي تنتهي تمتلئ مداراتها جميعها ما عدا المستوى الأخير، والغازات الخاملة.
- العناصر الانتقالية الرئيسية: وهي العناصر التي تمتلك نقصاً في عدد الإلكترونات في المستويين الأخيرين.
- العناصر الانتقالية الداخلية:وهي العناصر التي تمتلك نقصاً في الإلكترونات في مداراتها الثلاثة الأخيرة.
تدرج الصفات في الجدول الدوري
نصف قطر الذرة
يعرّف نصف قطر الذرة بالمسافة بين نواتي ذرتين في الجزيء الذري في الرابطة التساهمية أي التشاركية، وفي الأيونين في الرابطة الأيونية بين فلز ولا فلز، وتختلف المسافة تبعاً لتصنيف العناصر في الجدول الدوري على النحو الآتي:
- يقلّ نصف القطر في الدورة الواحدة كلّما زاد العدد الذري، أي كلما اتجهنا يميناً في الجدول الذري، والسبب في ذلك هو زيادة الشحنة الموجبة للنواة، ممّا يزيد من قوّة جذبها فيقلّ القطر بين الذرتين.
- يزداد نصف القطر في المجموعة الرأسية كلّما زاد العدد الذري، بسبب زيادة مستويات الطاقة في الذرة والتي تعمل على حجب تأثير النواة على الإلكترونات الخارجية فيقلّ التجاذب فيما بينها، وتزداد قوّة التنافر.
- نصف قطر الأيون الموجب أقلّ من نصف القطر للذرة المتعادلة في الفلزات، وذلك لأنّ الشحنة الموجبة للنواة تجذب الإلكترونات نحوها فيقلّ نصف القطر.
- نصف قطر الأيون السالب أكبر من نصف قطر الذرة المتعادلة في اللافلزات؛ لأنّ الشحنة السالبة للإلكترونات تزيد من قوة التنافر في الأيون.
جهد التأين
جهد التأين هو مصطلح يدل على مقدار الطاقة اللازمة لفصل أقلّ الإلكترونات ارتباطاً بالذرة، وتتغيّر بتغيّر موقع العنصر في الجدول الدوري كالآتي:
- يزداد جهد التأيّن في الدورة الواحدة بزيادة العدد الذري، بسبب زيادة الشحنة الموجبة التي تزيد من ارتباط الإلكترونات في الذرة.
- يقلّ جهد التأيّن في المجموعة الرأسية بزيادة العدد الذري، بسبب زيادة مستويات الطاقة التي تحجب قوّة جذب النواة.
- جهد التأين الأول للغازات الخاملة كبير جداً، أي أنّ الطاقة اللازمة لإزالة أول إلكترون من مداراتها كبيرة بسبب اكتمال المدارات واستقرارها.
- جهد التأين الثاني لأي عنصر أكبر من جهد التأين الأول له، بسبب زيادة قوة جذب النواة، بالإضافة إلى أنّ إزالة إلكترون ثانٍ قد تتسبب في كسر مستوى طاقة.
المقال السابق: عمل كنافة الشعر
المقال التالي: عمل كعك يمني
تصنيف العناصر في الجدول الدوري: رأيكم يهمنا
0.0 / 5
0 تقييم
